Hinweise zum Einsatz der Animation im Unterricht
Screenshots veranschaulichen die Funktionen der interaktiven Flash-Animation. Während der Präsentation werden die Reaktionsgleichungen an der Tafel fixiert.
Funktionen und Steuerung der Animation
Beschriftung der Zelle
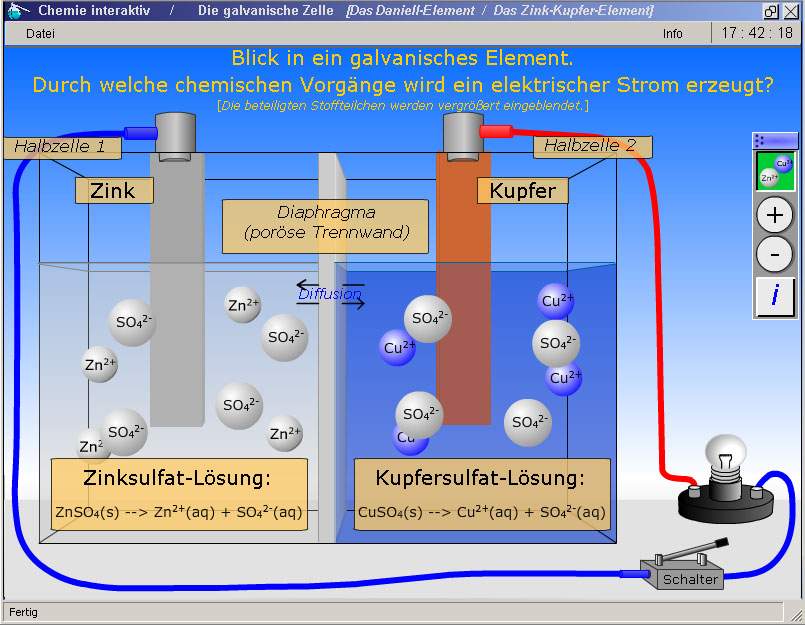
Die Animation beginnt die Präsentation mit einem Einblick in den Aufbau und die chemische Zusammensetzung eines galvanischen Elements. Ein Zinkblech taucht in eine Zinksulfatlösung und ein Kupferblech in eine Kupfersulfatlösung ein. Beide Systeme (Halbzellen) sind durch ein poröses Diaphragma voneinander getrennt (kombiniert). Die Beschriftung der Darstellung (Abb. 1, Platzhalter bitte anklicken) lässt sich über das obere Icon in der Buttonleiste (rechts außen) ein- beziehungsweise ausblenden.Stromfluss
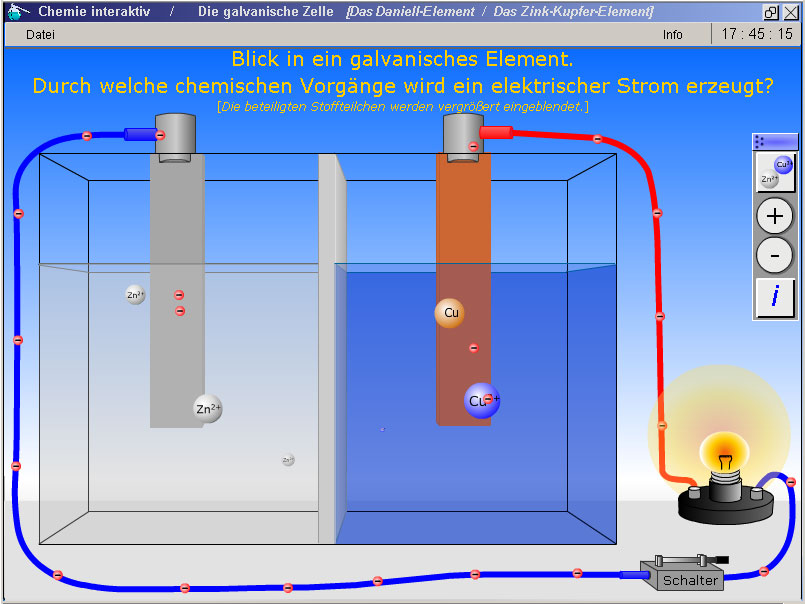
Durch Anklicken des Schalters (rechts unten in Abb. 2) wird der Stromkreis geschlossen (alternativ über die Space-Taste). Durch ein erneutes Anklicken des Schalters wird der Stromkreis unterbrochen und die Teilchensymbole werden ausgeblendet. Bei geschlossenem Stromkreis stoppt die Space-Taste die Bewegung der Teilchensymbole beziehungsweise startet sie bei erneuter Betätigung. Die Animation zeigt die chemischen Vorgänge an den Metallblechen (Elektroden) und den dadurch entstehenden Stromfluss. Die leuchtende Glühlampe zeigt den Verbrauch elektrischer Energie an. Anhand der projizierten Animation lassen sich die Teilgleichungen sowie die Redoxgleichung für den Gesamtumsatz an der Tafel entwickeln. Um jeder Schülerin und jedem Schüler die Elektrodenvorgänge deutlich vor Augen zu führen, lässt sich die Animation nach dem Stoppen über die Space-Taste mithilfe der Pfeil-Tasten langsam vor- oder zurückspulen. So kann jeder Elektrodenvorgang in angemessenem Tempo visualisiert werden. Die Teilvorgänge werden parallel zu diesem Vorgehen an der Tafel fixiert.Anode: Zinkatome werden oxidiert
In der Zinkhalbzelle werden Zinkatome oxidiert und gehen als Zink-Ionen in Lösung. Dabei werden zwei Elektronen über das Zinkblech zum Verbraucher abgeführt: Zn (s) → Zn2+ (aq) + 2e-Kathode: Kupferionen werden reduziert
In der Kupferhalbzelle werden dem Kupferblech zugeführte Elektronen auf die Kupferionen der Lösung übertragen. Durch die Reduktion dieser Kupferionen scheidet sich elementares Kupfer auf der Kathodenoberfläche ab: Cu2+ (aq) + 2e- → 2 Cu (s)
Ladungstransport und "Alterung"
Darstellung des Ladungstransports
Die Animation zeigt neben den Reaktionen an den Elektroden auch die Diffusion von Ionen durch das Diaphragma und damit den Ladungstransport in der Lösung, der die Aufrechterhaltung der Elektroneutralität in beiden Halbzellen gewährleistet. Die Erzeugung elektrischer Energie findet nur statt, wenn der Transport elektrischer Landungen im gesamten System (im gesamten Stromkreis) möglich ist: im metallischen Leiter und im Elektrolyten. Da positiv geladene Kupferionen an der Kupferelektrode entladen werden, wandern negativ geladene Sulfationen in die Zinkhalbzelle. Gleichzeitig wandern positiv geladene Zinkionen aus der Zinkhalbzelle in die Kupferhalbzelle."Alterung" des Galvanischen Elements
Durch die Veränderungen an den Elektroden (die allerdings in der Animation nicht gezeigt werden) lässt sich die Alterung des apparativen Systems erläutern und die Stromabnahme prognostizieren.Zurück
- Funktion einer galvanischen Zelle
Dieser Link führt Sie zurück zur Startseite der Unterrichtseinheit.