Das Molekulare Elektrostatische Potenzial (MEP)
Für die Darstellung der Ladungsverteilung auf den Moleküloberflächen wurden Berechnungen des Molekularen Elektrostatischen Potenzials (MEP) verwendet. Was sagt diese Größe genau aus?
Wie wohl fühlt sich eine Ladung?
Der Zusammenhang zwischen elektronischer Struktur und chemischer Reaktivität einer Verbindung lässt sich besonders gut durch das Molekulare Elektrostatische Potenzial (MEP) erschließen. Wie der Name bereits sagt, drückt das MEP eine Potenzialdifferenz, also ein Spannungsunterschied zwischen zwei Orten aus. Das heißt, es wird die Energie an einem Punkt im Raum bestimmt, die dort eine Probeladung (positive Einheitsladung) erfährt, wenn man sie aus dem Unendlichen an diesen Punkt bringt. Oder anschaulicher: Es wird bestimmt, wie "wohl" sich diese positive Ladung an diesem Punkt fühlt. Das MEP berechnet sich an diesem Ort vereinfacht durch Summation der Wechselwirkung aller Ladungen qi im Molekül mit dieser Probeladung. Das MEP drück eine Energie aus, was prinzipiell einer Spannungsdifferenz (in Volt) entspricht. Verbreiteter ist aber die Angabe in Kilokalorien pro Mol oder Kilojoule pro Mol.
MEP gleich Ladungsverteilung?
Rote Bereiche - Elektronenüberschuss
Für die Einfärbung der Moleküle wurde das MEP für alle Punkte auf einer Moleküloberfläche berechnet und diese entsprechend eingefärbt. Die Farbskala erstreckt sich dabei von Rot bis Blau. Rote Bereiche stellen in den Jmol-Applets Bereiche mit stark negativem MEP dar (Elektronenüberschuss), also Bereiche, in denen sich positive Ladungen "wohl" fühlen.Blaue Bereichen - Elektronendefizit
In blauen Bereichen ist das MEP positiv und es herrscht ein Elektronendefizit; positive Ladungen fühlen sich hier "unwohl", aber negative Ladung halten sich dort "sehr gern" auf. Die Farbgebung ist programmabhängig und daher willkürlich. Das MEP ist - streng genommen - nicht gleich der "Ladungsverteilung", als die es in den Folien deklariert wird. Dieser Begriff ist jedoch der für Schülerinnen und Schüler anschaulich und erlaubt ihnen, über die MEP-Färbung den Reaktionsverlauf besser zu verstehen.Ausblick in die Physik - für Experten
Das Coulomb-Gesetz
Grundlage des MEP bildet das Coulomb-Gesetz, welches die Wechselwirkungsenergie zweier Ladungen (Partialladungen) qi und qj mit Abstand rij zwischen den beiden Ladungen i und j unter Einbeziehung der Dielektrizitätskonstanten des umgebenden Mediums ε beschreibt:

Varianten der MEP-Darstellung
Durch Berücksichtigung beziehungsweise Addition aller Wechselwirkungsenergien der Ladungen i in einem Molekül - oder auch zwischen mehreren Molekülen - mit der Probeladung j errechnet sich das MEP am Ort der Probeladung. Die Visualisierung des MEP basiert auf den berechneten Werten und ist in zwei Varianten möglich:Moleküloberfläche
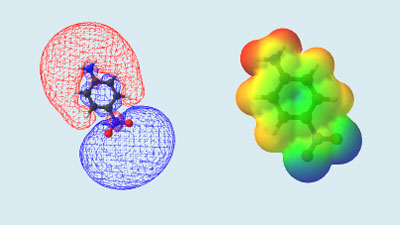
Auf einer Moleküloberfläche, zum Beispiel der van-der-Waals-Oberfläche oder der eines Kalottenmodells, werden die unterschiedlichen MEP-Werte in verschiedenen Farben projiziert. Diese Variante verwenden wir bei der Darstellung der Reaktionsmechanismen. Im Falls von p-Nitroanilin ist die Aminogruppe rot, also positiv, und die Nitrogruppe blau, also negativ polarisiert (Abb. 9, rechts).Isooberfläche
Auf einer Isooberfläche (ähnlich einer Isobarenkarte beim Wetter) wird ein bestimmter MEP-Wert - zum Beispiel +/-10 Kilokalorien pro Mol - ausgewählt. Dann werden alle Punkte im Raum mit diesem Potenzial durch eine dreidimensionale Isopotenzialoberfläche verbunden (Abb. 9, links). Somit ist der Abstand der Fläche zu den Atomen nicht mehr äquidistant wie bei einer Moleküloberfläche (Abb. 9, rechts). Im Beispiel des p-Nitroanilin ist das Isokonturlevel bei +10 rot und bei -10 Kilokalorien pro Mol blau.
Zurück
- Reaktionsmechanismen der Organischen Chemie in 3D
Über diesen Link gelangen Sie zurück zur Startseite des Artikels.